コン タム教授、ピーター マッカラムがんセンター
臨床試験とは?
臨床試験は健康研究の重要な部分です。 臨床試験は、新しい治療法、技術、検査、または新しい治療方法に関する重要な質問に答える管理された方法です。 臨床試験では、次のような質問をします。
- 新薬の安全性と有効性
- 標準治療への新しい薬の追加
- 標準治療の新しい方法を検討中
- 新しい治療法と古い治療法を比較して、どちらが副作用が少なく、より良い結果をもたらすかを確認します
現在使用が承認されている優れた治療法は、長年にわたる実験室および臨床研究の結果です。
臨床試験を実施する際の最も重要な要素は、参加している患者の安全と健康です。 オーストラリアでのすべての臨床試験は、さまざまな委員会によって厳密に審査および承認されており、試験が科学的および倫理的に健全であり、オーストラリアのすべての規制要件を満たしていることが保証されています。 これらの審査は、臨床試験に患者を登録する前に完了する必要があります。
臨床試験は、国の倫理ガイドラインと行動規範によって管理されています。 要件の詳細については、 ヒト研究における倫理的行為に関する国家声明 と オーストラリアの責任ある研究行動規範。
承認されていない物質およびデバイスの臨床試験は、TGA が採用するように、Therapeutic Goods Administration (TGA) の要件および国際ガイドラインに準拠する必要があります。 Therapeutic Goods Administration (TGA) は、オーストラリアで販売されるすべての医薬品を規制するオーストラリア政府の部門です。 臨床試験で使用されるすべての実験薬は、TGA に登録する必要があります。 詳細については、次を参照してください。 tga.gov.au。
臨床試験は、製薬会社、TGA や FDA などの国内外の規制機関による審査と監査の対象となります。
臨床試験の承認と実施の厳格な方法により、参加者の安全と権利が保護され、収集されたデータが高品質であることが保証されます。
ジュディス・トロットマン教授、コンコード病院
臨床試験はどのように設計されていますか?
臨床試験は、参加している患者さんにとって公正かつ安全であるように、科学的な方法で設計されています。
新しい薬や治療法をテストするには長い時間がかかります。 治療法が人で試される前に、科学者と医師は実験室での研究に何年も費やしました。 新しい治療法を段階的にテストする計画が立てられています。 各試験の結果は、次のフェーズに進む前に分析されます。
臨床試験には 4 つのフェーズがあります。
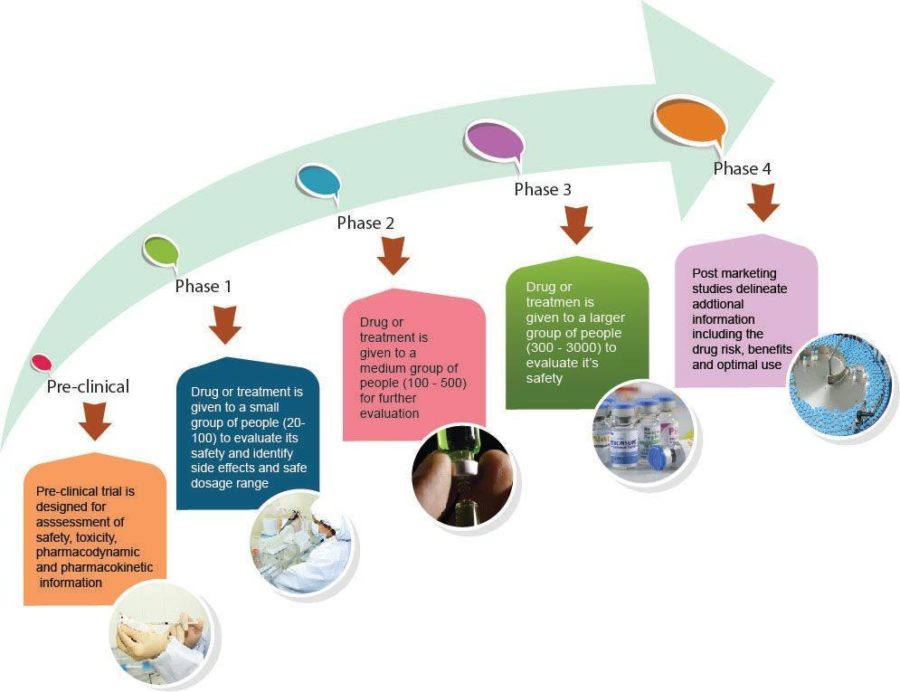
| 目的 | 実施方法 | |
| フェーズI | 安全性プロファイルと副作用を評価する 後の段階の試験でさらに検討される安全な用量を確立する | 非常に少数の参加者 (20-50) 新薬の治験では、通常、参加者には非常に少量の用量が与えられ、この用量が安全であることが確認されたら、次の参加者グループでは用量を増やします。 多くの場合、参加者は血液検査、心臓検査などの追加検査を受ける必要があります。 |
| フェーズ2 | 安全性プロファイルをさらに見る 薬の投与量が病気に対してどの程度効果があるかを詳しく調べる | 第1相試験よりも大きな数 (100-500) |
| フェーズ3 | この段階では、新しい薬や治療法を現在の治療法と比較します | 多数の参加者が登録 (300 以上) |
| フェーズ4 | 薬の使用が承認されると、これらの試験は、一般集団における承認された薬の有効性を監視するように設計されています | 非常に多くの参加者 |
ランダム化とはどういう意味ですか?
試験が治療法を互いに比較する場合、多くの場合、試験は無作為化されます。 つまり、トライアルへの参加に同意すると、コンピューターがランダムに治療方法の XNUMX つに割り当てます。 治療はしばしば「治療群」と呼ばれます
あなたも主治医も、あなたに割り当てられる治療群を選択することはできません。 このプロセスは、試験が公平であり、各グループの結果が科学的に比較できることを保証するために使用されます。
目くらまし とはどういう意味ですか?
ブラインドとは、参加者が受けている治療の性質を隠す行為を指します。 一部の試験では、参加者がどの治療を受けているか分からないように盲検化されています。 これはブラインドトライアルとして知られています。 盲検臨床試験では、参加者は自分が研究のどのアームにいるかを知りません。盲検化の目的は、利益と副作用の報告における偏りを減らすことです。
プラセボとは何ですか?
プラセボは、非アクティブまたは模擬治療です。 試験中の治療のように見える、味わう、または感じるように作られています。 違いは、有効成分が含まれていないことです。 プラセボは、結果が実際の治療によるものであることを確認するために使用されます。 プラセボを使用する場合は、標準治療に追加されます。 プラセボ治療自体はありません。 例えば、標準的な治療と実験的な治療を受けることができます。 標準治療とプラセボを受けることができます。
参加している治験でプラセボが使用されているかどうかは常に通知されます。 実験的治療を受けているかプラセボを受けているかはわかりません。
Michael Dickinson 博士、Peter MacCallum Cancer Center
臨床試験では何が行われますか?
臨床試験は、事前に設定された計画またはプロトコルに従って実施されます。 プロトコルは、どの患者を試験に登録できるか、どの検査が必要か、どのような治療が必要か、どのようなフォローアップが必要かを規定しています。 臨床試験に登録するとどうなるかについて詳しく読むことができます。
インフォームド・コンセントとはどういう意味ですか?
臨床試験に登録する前に、同意書に署名する必要があります。 このプロセスは非常に重要です。 参加は完全に任意です。 いかなる人も、臨床試験への参加を強制または圧力を受けるべきではありません。 医師と治験チームが治験について詳しく説明します。 彼らはあなたが書面による情報シートを持っていることを確認します。 情報を読み、参加するかどうかを考える十分な時間が与えられます。 参加することのメリットとリスクを含め、何が含まれるかを十分に理解することが重要です。 一部の臨床試験では、追加の予約と検査が必要になる場合があります。 これらはすべて説明され、情報シートに記載されます。 これについては、家族、友人、またはかかりつけの医師と時間をかけて話し合うことができます。 臨床試験に参加する必要はありません。 それは完全にあなたの決定であり、あなたが参加したくない場合は医師が理解しています. 参加しないことを決定した場合は、現在利用可能な治療を受けます。
参加が決定したら、同意書に署名する必要があります。 これはあなたの医者と一緒に行われます
臨床試験の適格性とはどういう意味ですか?
参加に同意し、同意書に署名したら、トライアルが自分に適していることを確認するプロセスを開始します。 これは、適格基準の完了として知られています。 これらは、参加者ができるだけ似ていることを確認するために満たす必要がある要件です。 適格性を満たしていないために試験が適切でない場合は、医師が他の選択肢について話し合います。
治療
すべての適格基準が評価され、試験があなたに適している場合は、治療グループが割り当てられます. 治療期間中は、定期的に通院して治療と検査を行います。 追加の訪問を行い、追加の検査を受ける必要がある場合があります。 また、自分の気持ちについての質問に答える必要があるかもしれません。 医師、看護師より説明を受けます。 この情報は、治験に同意する前に受け取った情報シートにも記載されています。 与えられたすべての指示に従うことが重要であり、質問がある場合は医師または看護師に連絡してください。
フォローアップケア
治療が完了すると、フォローアップとして知られるフェーズに移行します。 医師と看護師の診察を受け、追加の検査が必要になる場合があります。 たとえば、血液検査、心臓検査、アンケートなどです。
臨床試験からの撤退
臨床試験に参加したくないと判断した場合は、説明なしでいつでも参加できます。 これについて罰せられることはありません。 同意を撤回した場合は、現時点で最適な標準治療を受けることになります。
臨床試験を見つける方法は?
あなたの医師は、あなたに適した臨床試験について知っています。 主治医が臨床試験について話してくれず、参加に興味がある場合は、利用可能なものがあるかどうか主治医に尋ねることができます。 また、旅行したい他の病院に試験があるかどうかを尋ねることもできます。 あなたが尋ねても、あなたの医者は気分を害することはありません。
臨床試験について知ることができる場所がいくつかあります。
医療チーム
最初のステップは、どのような選択肢があるかについて医師に相談することです。 あなたに適した利用可能な臨床試験があるかどうかを尋ねる必要があります. 主治医は、あなたとあなたの病歴を最もよく知っています。 彼らは通常、あなたの病院、地域、州間高速道路に適したものがあるかどうかを知っています。 利用可能な臨床試験について知らない場合は、オーストラリア中の他の医師に、試験について知っているかどうか尋ねることができます.
セカンドオピニオン
もう XNUMX つの選択肢は、別の医師にセカンドオピニオンを求めることです。 多くの患者さんがセカンドオピニオンを求めます。 ほとんどの医師もこれに満足しているので、気分を害する心配はありません. ほとんどの医師は、あなたの命が重要であることを理解しています。
臨床試験参照
これは、臨床試験研究への参加を増やすために設計されたオーストラリアの Web サイトです。 すべての患者、すべての治験、すべての医師が利用できます。 目的は次のとおりです。
- 研究ネットワークの強化
- 紹介者とつながる
- 治験への参加を治療オプションとして組み込む
- 臨床研究活動に違いをもたらす
- アプリ版もあります
ClinicalTrials.gov
ClinicalTrials.gov は、世界中で実施された民間および公的資金による臨床研究のデータベースです。 患者は、リンパ腫のサブタイプ、試験(既知の場合)、国を入力すると、現在利用可能な試験が表示されます。
オーストラリア白血病およびリンパ腫グループ (ALLG)
ALLG & 臨床試験
ケイト・ハルフォード、ALLG
Australasian Leukemia & Lymphoma Group (ALLG) は、オーストラリアとニュージーランドで唯一の非営利の血液がん臨床試験研究グループです。 ALLG は、「より良い治療…より良い生活」という目的に基づいて、臨床試験の実施を通じて、血液がん患者の治療、生活、生存率を改善することに取り組んでいます。 国内外の血液がんの専門家と協力して取り組んでいる彼らの影響は深刻です。 メンバーは血液学者であり、世界中の同僚と協力するオーストラリア全土の研究者です。
血液がん研究 西オーストラリア
A/Prof Chan Cheah、Sir Charles Gairdner Hospital、Hollywood Private Hospital & Blood Cancer WA
白血病、リンパ腫、骨髄腫の研究を専門とする、西オーストラリアの血液がん研究センター。 彼らの目的は、血液がんの WA 患者に、命を救う可能性のある新しい治療法をより迅速に提供することです。
臨床試験はこれを達成するための最良の方法であり、パースの XNUMX つの拠点、サー チャールズ ガーディナー病院、リニア クリニカル リサーチ、ハリウッド プライベート病院で実施されています。
オーストラリアがん試験
このウェブサイトには、現在新しい参加者を募集している試験を含む、がん治療における最新の臨床試験を表示する情報が含まれ、提供されています。
ピーターマッカラムがんセンター
ピーター・マッカラムがんセンターは世界クラスのがんセンターです。 これらはオーストラリア最大のがん研究センターであり、750 名を超える研究室および臨床研究スタッフを擁しています。 臨床試験と資格の詳細については、Web サイトで確認できます。
オーストラリア ニュージーランド臨床試験登録
Australian New Zealand Clinical Trial Registry (ANZCTR) は、オーストラリア、ニュージーランドなどで実施されている臨床試験のオンライン レジストリです。 ウェブサイトにアクセスして、現在募集中の治験を確認してください。
リンパ腫連合
Lymphoma Coalition は、リンパ腫患者グループの世界的なネットワークであり、2002 年に設立され、2010 年に非営利団体として法人化されました。その明確な目的は、世界中で情報の公平な競争の場を作り、リンパ腫患者団体のコミュニティを促進することです。リンパ腫患者が必要なケアとサポートを受けられるようにするための努力を互いに支援すること。
一貫性と信頼性の高い最新情報の中心的なハブの必要性、およびリンパ腫患者組織がリソース、ベスト プラクティス、ポリシーと手順を共有する必要性が認識されました。 これを念頭に置いて、83 つのリンパ腫組織が LC を開始しました。 現在、52 カ国から XNUMX のメンバー組織があります。
参加したい試験が見つかったら、医師に適格基準を満たしているかどうかを尋ねてください。もしそうであれば、医師があなたの関与を調整したり、研究チームと連絡を取ったりできるかどうかを尋ねてください。
臨床試験に参加するメリットは何ですか?
臨床試験に参加することの主な利点は、臨床現場ではまだ利用できない新しい治療法や、自分の状況では利用できない既存の治療法を受けることができることです。 たとえば、ある人が特定のタイプのリンパ腫に対して標準的な治療を受けていて、望ましい反応が得られなかった場合、臨床試験は良い選択肢かもしれません。 研究的治療は、臨床試験以外の人には利用できません。 オーストラリアの人々に治療が施されるには、厳密に研究およびテストされ、Therapeutic Goods Administration (TGA) によって承認されなければなりません。 TGA は政府機関であり、すべての治療グッズを評価および監視して、オーストラリアのコミュニティが利用できるようになる前に、それらが許容できる基準であることを確認します。
臨床試験に参加するリスクは何ですか?
臨床試験に参加する前に、リスクを認識しておく必要があります。 それらには以下が含まれます:
- 治療は有毒である可能性があり、重度または未知の副作用が発生する可能性があります
- この治療法は、標準的な治療法よりも効果が低く、利益がほとんどまたはまったくないことが判明する可能性があります
- あなたは臨床試験の対照群に属している可能性があり、そのため、実験的治療ではなく標準的なリンパ腫治療を受ける可能性があります
医師に尋ねるべき質問
- この臨床試験の目的は何ですか?
- 研究はどのくらい続きますか?
- 研究に参加したほうがよいでしょうか?
- この研究は私の日常生活にどのような影響を与える可能性がありますか?
- 研究に参加するのに費用はかかりますか?
- 私の病気の患者は全員、この治験に参加できますか?
- 治験に参加した場合、最善の治療を受けることはできませんか?
臨床試験を理解する - Lymphoma Australia のビデオ
ジュディス・トロットマン教授、コンコード病院
Michael Dickinson 博士、Peter MacCallum Cancer Center
コン タム教授、ピーター マッカラムがんセンター
Eliza Hawkes 博士、Austin Health & ONJ がん研究センター
Eliza Hawkes 博士、Austin Health & ONJ がん研究センター
ケイト・ハルフォード、ALLG
A/Prof Chan Cheah、Sir Charles Gairdner Hospital、Hollywood Private Hospital & Blood Cancer WA
募集中の臨床試験
臨床研究:再発または難治性の古典的ホジキンリンパ腫(TIRHOL)の参加者に対するチスレリズマブ[2021年XNUMX月時点]
情報源
ヒト研究における倫理的行為に関する国家声明 (2007) (国家声明 (2007) は、1992 年の国家保健医療研究評議会法に従って作成された一連のガイドラインで構成されています。
オーストラリアの責任ある研究実施規範、2018 年
カン・J・サーグ。 2010 10月; 53(5):345 - 348。
Blinding: 誰が、何を、いつ、なぜ、どのように?
ポール・J・カラニコラス、MD、PhD、*† フォーラフ ファロキャル、MPhil、PhD、†‡および モーヒト・バンダーリ、MD、MSc

